
Il Deficit di biotina, la vitamina B8, ha implicazioni possibili attraverso la reazione metabolica all'interno del nostro corpo.
Anche se è abbastanza raro, è un disordine nutrizionale al quale, dandogli il permesso di andare incontrollato o non trattato può diventare una condizione molto grave.
La forma più grave, è fatale. Può verificarsi in qualsiasi fascia di età, sia nei maschi che nelle femmine e in qualsiasi parte del mondo.
La biotina è una vitamina idrosolubile, minerali e vitamine liquidi possono aiutare questo processo nutrizionale di assimilazione, semplicemente a causa della loro rapporto di assorbimento superiore e di esatto fabbisogno per nostro corpo. Questa preziosa sostanza nutritiva è generalmente classificata come una vitamina del complesso B: la Vitamina B8.
Dopo la scoperta iniziale dell’esistenza della biotina, diversi suo vantaggi iniziarono ad emergere. Quasi quaranta anni di ricerche sono state eseguite prima che fosse stata classificata come una vitamina. Questa sostanza nutritiva è utile, guasi indispensabile per tutti gli i organi e può essere sintetizzata da:
- Batteri
- lieviti,
- muffe
- alghe e alcune piante.
Nella sua forma attiva, la biotina è collegata alla sintesi attiva di quattro importantissimi enzimi noti come carboxylases. Anche se ancora non vi è molta conoscenza nelle comunità scientifica sulle vitamine idrosolubili, effettivamente in qualità di modulatori genetici, è noto che questi enzimi partecipano al metabolismo dei carboidrati, lipidi e proteine e fanno da catalizzatori.
In poche parole, il processo di catalizzatori degli enzimi significa che gli enzimi agiscono diminuendo i livelli di energia o l'energia di attivazione, e questo costituisce una reazione. Questa reazione a sua volta aumenterà notevolmente la velocità di reazione. Ogni gruppo di carboxylase catalizza una reazione metabolica essenziale all'interno del vostro corpo, questo è stato riscontrato come essere il principale vantaggio della biotina all'interno del nostro corpo.
Queste reazioni metaboliche includono la sintesi degli acidi grassi, la formazione di glucosio da fonti diverse dai carboidrati; per esempio gli amminoacidi e grassi, il metabolismo della leucina, un aminoacido essenziale e il metabolismo del colesterolo.
Anche se il deficit di questa sostanza nutritiva è molto raro, l'esigenza di biotina nella dieta umana ha dimostrato che il palese deficit e la mancanza di adeguate quantità di biotina può provocare i seguenti sintomi:
- perdita di capelli
- eruzione cutanea rossa squamosa intorno gli occhi, naso e bocca
- rash intorno alla zona genitale.
Sintomi neurologici negli adulti includono:
- depressione
- letargia
- allucinazione
- intorpidimento e formicolio delle estremità. (in alcuni casi)
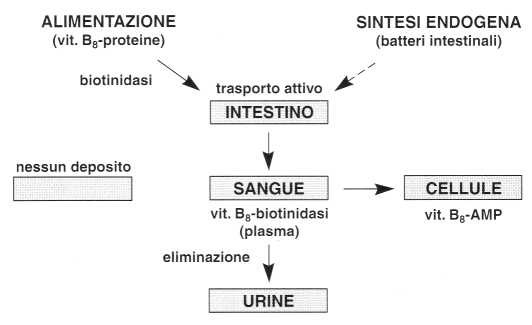
Deficit di biotinidasi è considerato una malattia ereditaria diagnosticata entro i primi mesi di vita nei neonati. I sintomi di questa malattia possono variare significativamente da caso a caso, ma nelle forme piu’ gravi, può causare:
- crisi epilettiche
- problemi respiratori
- un ritardo di sviluppo per il neonato.
Se non diagnosticato correttamente, può portare:
- una perdita di udito
- una perdita di visione
- eruzioni cutanee e atassia
che sono problemi con il movimento e fissaggio dell’ l'equilibrio
Se diagnosticato correttamente un trattamento immediato e permanente con supplementazione di biotina può prevenire queste condizioni.
Si consiglia di consultare sempre il medico circa gli integratori, soprattutto durante la gravidanza, una corretta assunzione di questa vitamina può impedire questo deficit ereditario.
È anche noto da anni che il deficit di Biotina alterata utilizzazione del glucosio. La Biotina è indicata per stimolare la glucochinasi, un enzima nel fegato, con conseguente maggior sintesi di glicogeno, che sarebbe il modulatore di stoccaggio del glucosio.
Le unghie fragili nell'uomo sono state attribuite anche alla mancanza di biotina.
La Biotina si trova in molti alimenti, ma generalmente in quantità inferiore rispetto alle altre vitamine idrosolubili.
Fonti di cibo ricche di biotina includono:
- il lievito, (panificatori attivi)
- la crusca di frumento (grezzo)
- il pane (grano intero)
- uova (cotte)
- formaggio (camembert)
- fegato (cotto)
- pollo (cotto)
- carne di maiale (cotta),
- salmone (cotto)
- avocado,
- lamponi,
- carciofi e cavolfiore (crudi).
Ci sono oramai in commercio diverse marche (ottime) di integratori liquidi che possono aiutare a prevenire la carenza di questa sostanza nutritiva.
Consultare sempre Medici e Specialisti del settore
Fonte: http://fetale-feto.blogspot.it/2011/08/deficit-di-biotina.html
.....................................................................................................................................................
Disordine dello sviluppo di tipo autistico: Deficit di biotina
Biotina e Biotinidasi
Casi clinici
Riportiamo il caso di un bambino con parziale deficit di biotinidasi e disordine dello sviluppo di tipo autistico.
Siamo arrivati alla diagnosi di deficit di biotinidasi quando il bambino aveva un'età di quasi 4 anni.
Di conseguenza, il paziente ha iniziato il trattamento con il cofattore biotina (10 mg/giorno), che però non ha risolto il suo comportamento autistico. Il suo fratello più giovane era anch'egli affetto da parziale deficit di biotinidasi, diagnosticato alla nascita grazie al nostro programma di screening neonatale. Il paziente è stato trattato precocemente con terapia con cofattore biotina (10 mg/giorno), e non ha mostrato alcuna anomalia comportamentale, né ritardi nello sviluppo.
Dato che il cervello è abbastanza vulnerabile al deficit di biotina, un ritardo nella terapia per mezzo di biotina potrebbe causare un danno neurologico. Il nostro paziente è il primo caso di deficit parziale di biotinidasi associato all'autismo. Ipotizziamo che la bassa attività della biotinidasi possa aver causato il deficit di biotina nel suo cervello e nel fluido cerebrospinale e, di conseguenza, seri problemi neurologici, come i comportamenti stereotipati ed autistici, che sono stati irreversibili nonostante il supplemento di biotina.
Descriviamo una nuova patologia dei gangli basali sensibile alla biotina in 10 pazienti.
All’inizio la patologia compare sotto forma di encefalopatia subacuta, con confusione, disartria e disfagia, con occasionale paralisi nervosa facciale sopranucleare od oftalmoplegia esterna, e progredisce verso una grave rigidità della ruota dentata, distonia e tetraparesi. Se viene somministrata biotina (5-10 mg/kg/giorno), questi sintomi scompaiono entro pochi giorni, e non vi sono sequele neurologiche. Queste ricompaiono entro un mese se la biotina viene interrotta. I pazienti diagnosticati tardi, o che hanno sofferto di episodi ripetuti, soffrono di sintomi residui quali paraparesi, leggero ritardo mentale o distonia. I numerosi studi biochimici sul metabolismo intermedio, come gli studi autoimmuni e tossicologici, ed i test enzimatici che includevano le attività lisosomiale, di biotinidasi e carbossilasi, e gli studi batterici e virali erano tutti normali. L’eziologia potrebbe essere correlata ad un difetto nel vettore della biotina attraverso la barriera sangue-cervello. L’unica anomalia radiologica coerente era una necrosi centrale della testa del caudato, con coinvolgimento bilaterale e completo, o parziale, del putamen alla risonanza magnetica del cervello. Questa necrosi era presente durante l’encefalopatia iniziale acuta e rimaneva invariata durante il follow-up di 3-10 anni. Sebbene la sua eziologia sia sconosciuta, è importante riconoscere questa patologia, perché i suoi sintomi possono essere annullati e la progressione del suo decorso clinico prevenuta semplicemente per mezzo dell’assunzione di biotina.
Vengono riportati gli studi biochimici in cinque pazienti con un difetto nella sintesi sensibile alla biotina della olocarbossilasi.
Sia l’età di inizio (da 2 a 6 anni) che la gravità della patologia variavano in maniera considerevole.
In tutti i pazienti la diagnosi è stata stabilita per mezzo della scoperta di aciduria organica, tipica dei deficit multipli della carbossilasi in uno stato catabolico. In quattro pazienti la risposta alla terapia con biotina è stata valutata per mezzo della misurazione delle attività della carbossilasi mitocondriale nei linfociti e per mezzo di monitoraggio delle escrezioni urinarie organiche acide. In tre pazienti i sintomi clinici sono scomparsi con un dosaggio di 10-20 mg biotina/giorno, mentre la normalizzazione dei parametri biochimici ha reso necessarie dosi più alte (20-40 mg/giorno).
La quarta paziente ha necessitato un dosaggio di 100 mg biotina/giorno prima che la sua eruzione cutanea scomparisse. La paziente rimane mentalmente ritardata e mostra escrezioni urinarie organiche acide leggermente elevate. In due pazienti le attività della carbossilasi erano chiaramente carenti nella crescita dei fibroblasti nel medium comunemente utilizzato, che contiene 10 nmol/L biotina (apportato nel medium da FCS). I fibroblasti degli altri tre pazienti sono diventati carenti solamente in un medium a bassa biotina (0,1 nmol/L).
La riattivazione delle attività carenti in carbossilasi in relazione al tempo ed alla concentrazione di biotina si correlavano bene con la severità e l’età dell’inizio della patologia in quattro pazienti. In un paziente, tuttavia, la riattivazione della carbossilasi ha seguito un modello più complesso, che ha reso necessario un tempo di incubazione più lungo, ma una concentrazione di biotina solo moderatamente aumentata, di 19 nmol/L rispetto ai 3-5 nmol/L delle cellule normali e 34-4000 nmol/L degli altri quattro pazienti.
I risultati nei cinque pazienti sono conformi ad un difetto primario della sintetasi della olocarbossilasi dovuto ad una affinità diminuita per la biotina, in un paziente combinata con una diminuzione del Vmax.
PMID: 9128289 [PubMed - indexed for MEDLINE]
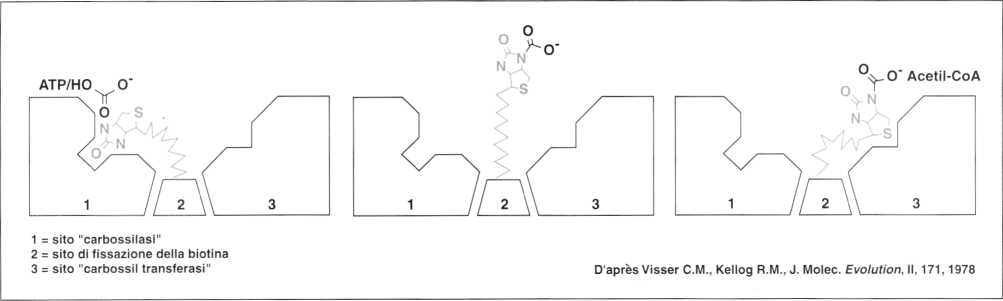
Per anni, il ruolo principale della biotina nell’essere umano è stato considerato essere solo quello di coenzima per quattro carbossilasi.
Sebbene siano state rilevate prove che la biotina potrebbe avere altre funzioni, nessuna di esse è stata accertata con sicurezza. La scoperta che il siero umano biotinidasi possiede un’attività di biotinil-transferasi, oltre a quella di idrolasi della biotinidasi, presenta nuove possibilità per il ruolo della biotinidasi nel metabolismo della biotina. Il trasferimento specifico della biotina agli istoni da parte della biotinidasi fornisce una possibile spiegazione del motivo per il quale la biotina viene rilevata nel nucleo, e della natura del suo ruolo nella regolazione della trascrizione delle proteine. Studi futuri aiuteranno a determinare le funzioni della biotinidasi nel metabolismo della biotina e negli stati patologici. PMID: 10064314 [PubMed - indexed for MEDLINE]
E’ stata misurata l’attività della lipoamidasi (cui non è ancora stato conferito un numero EC) in vari tessuti del ratto utilizzando due substrati differenti, uno naturale, la lipoil-lisina (epsilon-N-(D,L-lipoil)L-lisina) ed uno artificiale, l’acido lipoil-p-amminobenzoico (acido N-D,L-lipoil-p-amminobenzoico).
La biotinidasi, EC 3.5.1.12, è stata misurata nello stesso tessuto con un substrato artificiale, l’acido biotinil-p-amminobenzoico (acido N-D-biotinil-p-amminobenzoico).
La lipoamidasi misurata come attività di idrolasi dell’acido lipoyl-p-amminobenzoico aveva due livelli ottimali di pH, a pH 6,0 ed a pH 9,5, in fegato omogenato, ma solamente un livello ottimale di pH a pH 6,0 nel plasma del ratto.
La lipoamidasi misurata come attività di idrolasi della lipoil-lisina aveva un livello ottimale di pH a pH 5,5 sia nel fegato omogenato che nel plasma. Nello stesso modo, la biotinidasi mostra un singolo livello ottimale del pH a pH 6,0 sia nel fegato omogenato che nel plasma. Le proprietà dell’idrolasi della lipoil-lisina e della biotinidasi erano simili sia per termostabilità che per stabilità del pH e modelli di inibizione, e le loro proprietà differivano da quelle dell’idrolasi dell’acido lipoyl-p-amminobenzoico. Le attività di idrolasi della lipoil-lisina e della biotinidasi erano al massimo in rene, fegato e plasma sanguigno, mentre le attività di idrolasi dell’acido lipoil-p-amminobenzoico erano al massimo in fegato, cervello e rene. Le attività di idrolasi della lipoil-lisina e della biotinidasi sono state scoperte soprattutto nella frazione microsomiale del fegato, e l’idrolasi dell’acido lipoyl-p-amminobenzoico è stata ripresa dalla frazione microsomiale ed in parte dalla frazione mitocondriale. Questi risultati indicano che l’idrolasi dell’acido lipoil-p-amminobenzoico del fegato è una proteina enzimatica diversa dall’idrolasi lipoil-lisina, ed i dati indicano anche che l’idrolasi lipoil-lisina del fegato e la biotinidasi sono la stessa proteina enzimatica. PMID: 7981329 [PubMed - indexed for MEDLINE]
Viene descritta una purificazione di più di 20.000 volte del siero umano lipoamidasi.
Questa è stata effettuata per mezzo di precipitazione di (NH4)2SO4 e cromatografia su DEAE-Sepharose, Blue Sepharose CL-6B e fenil-Sepharose CL-4B, seguita da focalizzazione isoelettrica preparatoria (IEF) ed infine da cromatografia con permeazione di gel. La co-precipitazione e la co-cromatografia delle attività della lipoamidasi e della biotinidasi con identici rilasci e purificazione sono state ottenute a tutti i passi di purificazione, il che indica che le attività della lipoamidasi e della biotinidasi nel siero umano sono dovute alla stessa proteina enzimatica. Dopo la IEF preparatoria, sono state scoperte due frazioni con sua attività di lipoamidasi ed attività di biotinidasi, rispettivamente a pI 4,0 ed a pI 4,4. Abbiamo scoperto che la massa molecolare dell’enzima è di 76 kDa.
Quando come stabilizzatore durante la procedura di purificazione è stato utilizzato il 2-mercaptoethanol invece della cisteina, dopo la IEF preparatoria è stata ottenuta solamente una forma principale (pI 4,0) dell’enzima. Aggiungendo la cisteina, questa forma si è trasformata in un enzima con pI 4,4, il che indica che quest’ultima forma è un addotto della cisteina, prodotto durante la procedura di IEF. PMID: 8484735 [PubMed - indexed for MEDLINE]
E’ stato proposto un meccanismo enzimatico secondo il quale la biotinidasi potrebbe catalizzare la biotinilazione degli istoni.
Qui, si è scoperto che le cellule umane legano in maniera covalente la biotina agli istoni H1, H2A, H2B, H3 ed H4. Le cellule rispondono alla proliferazione con un aumento della biotinilazione degli istoni; la biotinilazione aumenta presto durante il ciclo cellulare e rimane ad alti livelli durante tutto il ciclo. Nonostante il ruolo di catalizzatore della biotinidasi nella biotinilazione degli istoni, la codifica della biotinidasi da parte dell’mRNA e l’attività della biotinidasi non corrispondevano all’aumento di biotinilazione degli istoni nelle cellule in proliferazione. La biotinilazione degli istoni potrebbe essere regolata da enzimi diverso dalla biotinidasi o dal tasso di de-biotinilazione degli istoni. PMID: 11606205 [PubMed - indexed for MEDLINE]
Fonte: Medline (Traduzione di Alessandra Torriani - torrianitrad@yahoo.it)
Bibliografia
Neuropsychol Dev Cogn Sect C Child Neuropsychol. 2003 Sep;9(3):184-8.
Caso di deficit parziale di biotinidasi associato ad autismo.
Zaffanello M, Zamboni G, Fontana E, Zoccante L, Tato L.
Centro Regionale per gli Errori Congeniti Neonatali del Metabolismo, Università di Verona, Verona, Italia
Brain. Luglio 1998 ;121 ( Pt 7):1267-79.
Patologia dei gangli basali sensibile alla biotina: una nuova entità.
Ozand PT, Gascon GG, Al Essa M, Joshi S, Al Jishi E, Bakheet S, Al Watban J, Al-Kawi MZ, Dabbagh O.
Dipartimento di Pediatria, Ospedale Specialistico King Faisal e Centro di Ricerca, Riyadh, Arabia Saudita. ozand@kfshr.edu.sa
Pediatr Res. Maggio 1997;41(5):666-73.
Cinque pazienti con un difetto sensibile alla biotina nella formazione della olocarbossilasi: valutazione della sensibilità alla terapia con biotina in vivo e studi biochimici comparativi in vitro.
Suormala T, Fowler B, Duran M, Burtscher A, Fuchshuber A, Tratzmuller R, Lenze MJ, Raab K, Baur B, Wick H, Baumgartner R.
Unità Metabolica, Ospedale Pediatrico Universitario, Basilea, Svizzera.
J Nutr. Giugno 1993;123(6):1140-9.
Deplezione e replezione di biotinil enzimi nel fegato di ratti con deficit di biotina: prove di un sistema di immagazzinaggio della biotina.
Shriver BJ, Roman-Shriver C, Allred JB.
Dipartimento di Scienza e Tecnologia Alimentare, Ohio State University, Columbus 43210, Ohio (USA).
J Nutr. Settembre 2001;131(9):2310-5.
L’assunzione dietetica di biotina modula l’insieme di biotina libera e legata alle proteine nel fegato del ratto.
Lewis B, Rathman S, McMahon R.
Dipartimento di Scienza Alimentare e Nutrizione Umana, Istituto di Scienze Alimentari ed Agricole, Università della Florida, Gainesville, 32611-0370, Florida (USA)
Int J Vitam Nutr Res. Luglio 2002;72(4):278-86.
Attività di carbossilasi dipendenti dalla biotina in diverse CNS e cellule derivate dalla pelle, e loro sensibilità alla deplezione di biotina.
Suormala T, Wiesmann UN, Cruz F, Wolf A, Daschner M, Limat A, Fowler B, Baumgartner ER.
Unità Metabolica, Ospedale Pediatrico Universitario, Romergasse 8, CH-4005 Basilea, Svizzera. Terttu.Suormala@unibas.ch
J Nutr. Febbraio 1999;129(2S Suppl):485S-489S.
La biotinidasi umana non serve semplicemente a riciclare la biotina.
Hymes J, Wolf B. Dipartimento di Genetica Umana, Medical College of Virginia presso la Virginia Commonwealth University, Richmond 23298, Virginia (USA).
Eur J Clin Chem Clin Biochem. Luglio 1994;32(7):501-9
Attività della lipoamidasi e della biotinidasi nel ratto: distribuzione tissutale e localizzazione intracellulare.
Nilsson L, Kagedal B.
Dipartimento di Chimica Clinica, Ospedale Universitario, Linkoping, Svezia.
Biochem J. 15 Aprile 1993; 291 ( Pt 2):545-51.
Co-purificazione del siero umano lipoamidasi e biotinidasi: prove del fatto che le due attività enzimatiche sono dovute alla stessa proteina enzimatica.
Nilsson L, Kagedal B.
Dipartimento di Chimica Clinica, Ospedale Universitario, Linkoping, Svezia.
Eur J Biochem. Ottobre 2001; 268(20):5424-9.
Biotinilazione degli istoni nelle cellule umane. Effetti di proliferazione delle cellule.
Stanley JS, Griffin JB, Zempleni J.
Dipartimento di Pediatria, Divisione di Immunologia ed Allergia, Università dell’Arkansas per le Scienze Mediche, ed Istituto di Ricerca dell’Ospedale Pediatrico dell’Arkansas, Little Rock, Arkansas (USA).


